據(jù)國家藥監(jiān)局官網(wǎng)在2020年3月31日發(fā)布的公告顯示:自4月1日起�����,出口新型冠狀病毒檢測(cè)試劑����、醫(yī)用口罩、醫(yī)用防護(hù)服�����、呼吸機(jī)�����、紅外體溫計(jì)的企業(yè)向海關(guān)報(bào)關(guān)時(shí)必須提供國內(nèi)醫(yī)療器械注冊(cè)證明并符合進(jìn)口國的質(zhì)量標(biāo)準(zhǔn)要求�。
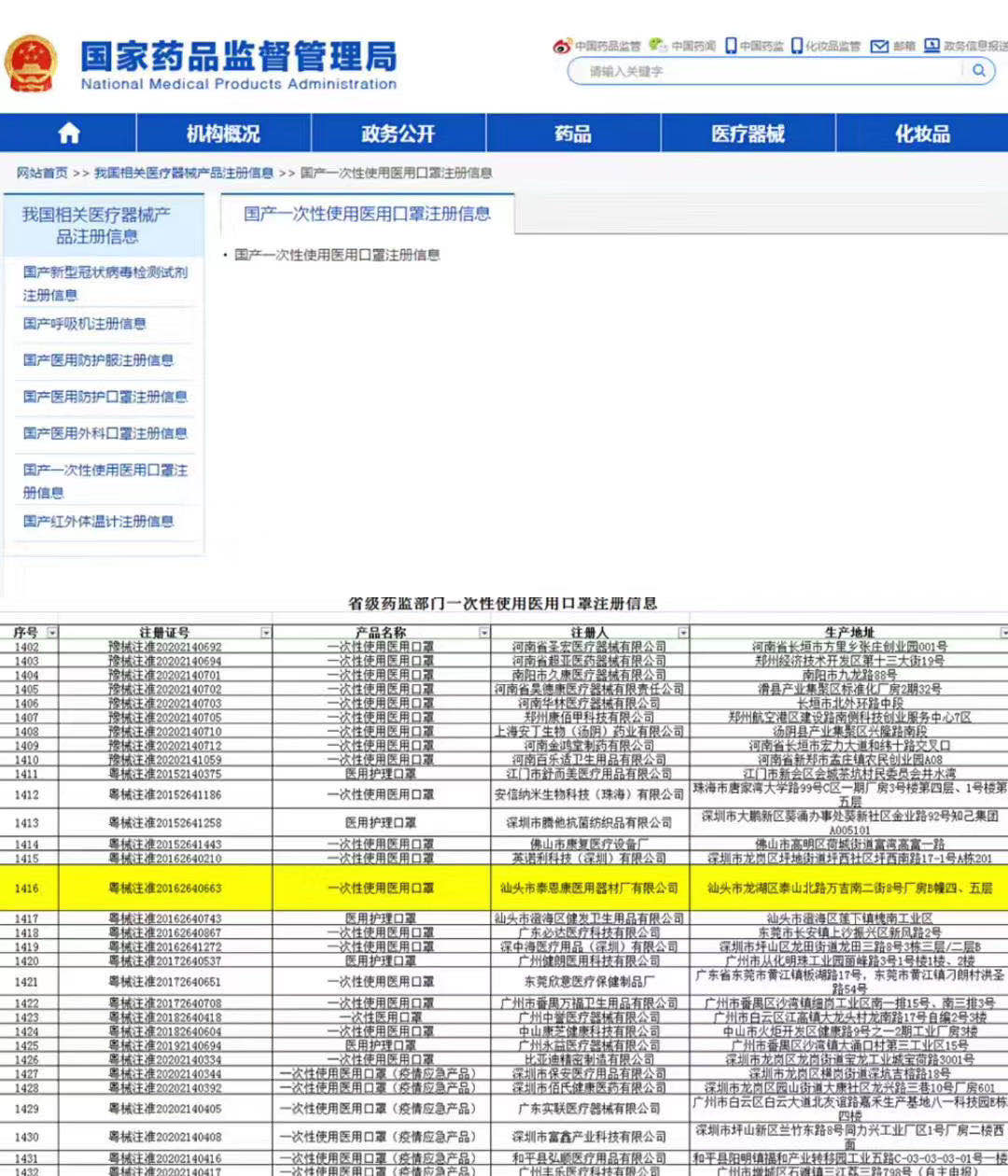
泰恩康一次性使用醫(yī)用口罩按國家相關(guān)法規(guī)和質(zhì)量標(biāo)準(zhǔn)申報(bào)注冊(cè),取得我國醫(yī)療器械產(chǎn)品注冊(cè)證書���,在國家藥品監(jiān)督管理局����,可查詢到相關(guān)注冊(cè)信息����。這意味著泰恩康一次性使用醫(yī)用口罩在中國持有合法醫(yī)療器械身份,且根據(jù)5號(hào)公告獲得出口白名單��。
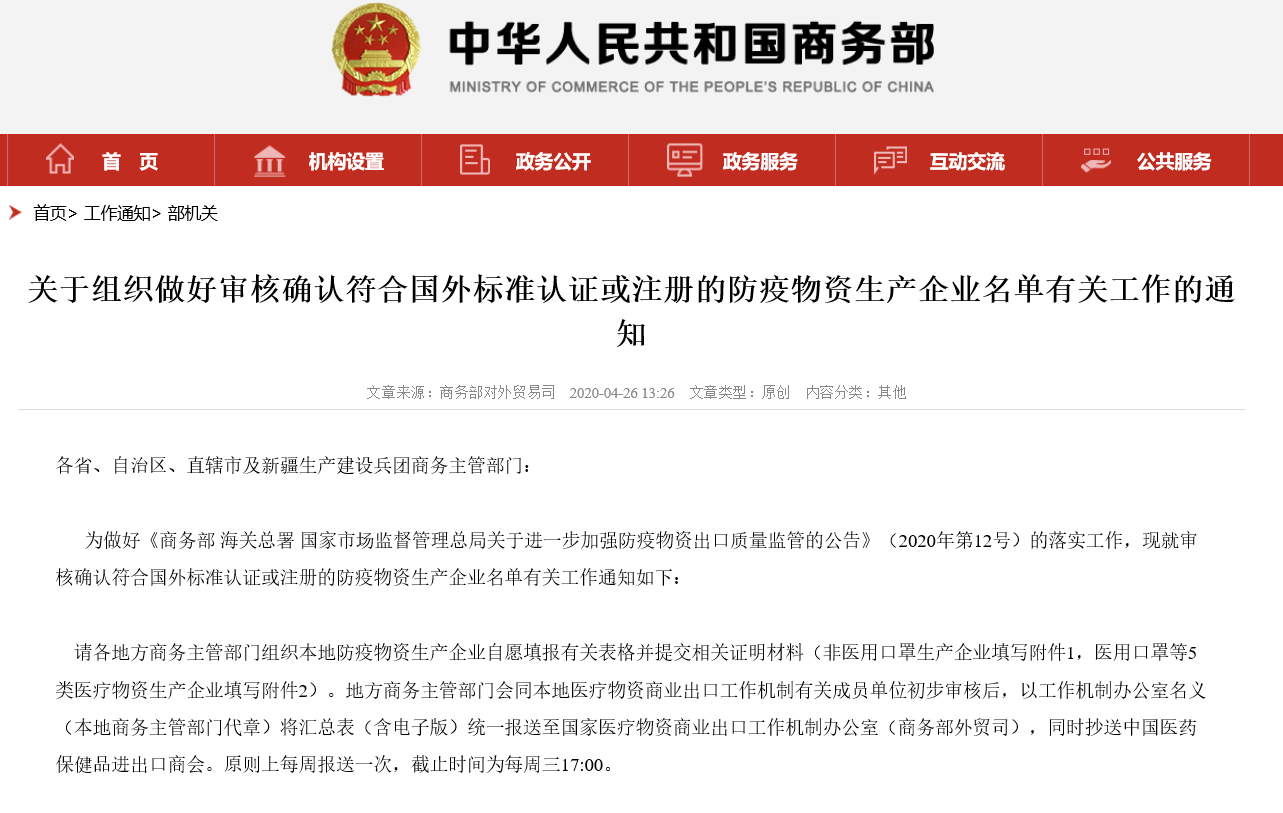
4月25日�,商務(wù)部會(huì)同海關(guān)總署和國家市場(chǎng)監(jiān)督管理總局��,三部門聯(lián)合發(fā)布2020年第12號(hào)公告���,緊急宣布進(jìn)一步加強(qiáng)防疫物資出口質(zhì)量監(jiān)管,加強(qiáng)非醫(yī)用口罩出口質(zhì)量監(jiān)管����,自4月26日起,出口的非醫(yī)用口罩應(yīng)當(dāng)符合中國質(zhì)量標(biāo)準(zhǔn)或國外質(zhì)量標(biāo)準(zhǔn)�。隨后,商務(wù)部發(fā)布通知:防疫物資生產(chǎn)企業(yè)可以向本地商務(wù)局申請(qǐng)加入商務(wù)部白名單���,并提交相關(guān)表格和證明材料�。在公布發(fā)出后�����,泰恩康第一時(shí)間做出反應(yīng)遞交申請(qǐng)材料��,5月8日���,泰恩康成功進(jìn)入中國商務(wù)部口罩CE出口白名單����。
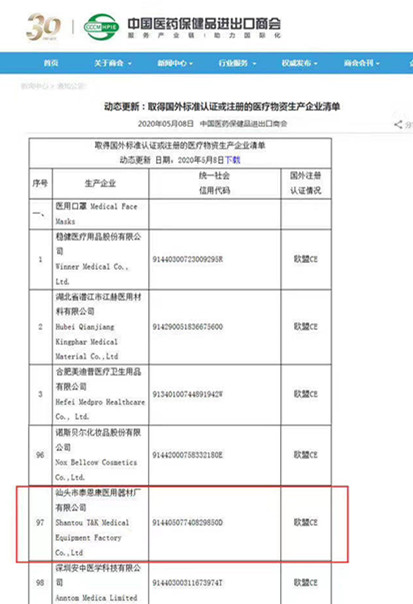
泰恩康連續(xù)入選5號(hào)公告及12號(hào)公告白名單,這意味著泰恩康醫(yī)用口罩取得商務(wù)部���、海關(guān)總署、國家市場(chǎng)監(jiān)督管理總局及國家藥品監(jiān)督管理局四大部門聯(lián)合認(rèn)同�,內(nèi)銷及出口都取得合法資質(zhì),“雙白名單”是國家與政府的認(rèn)可和信任�,也是泰恩康的責(zé)任。
今后泰恩康將一如既往地以精益求精的態(tài)度���,遵循“規(guī)?���;?、體系化”的發(fā)展思路,以市場(chǎng)為向?qū)?�,以質(zhì)量求生存�����,以管理促發(fā)展���,嚴(yán)格按照國家的法律法規(guī)����、相關(guān)國行標(biāo)準(zhǔn)的要求,著力于建造現(xiàn)代化的醫(yī)療器械生產(chǎn)基地���,再接再厲���,嚴(yán)控品質(zhì),輸送優(yōu)質(zhì)口罩系列產(chǎn)品���,力求為人們的健康事業(yè)做出卓著貢獻(xiàn)����。



